An Electric Car Battery That Will Get You From Paris to Brussels and Back
The metal-air battery carries more energy per kilogram than today’s lithium-ion batteries
By Winfried W. Wilcke & Ho-Cheol Kim
Posted 26 Feb 2016 | 17:00 GMT
 |
| Illustration: Elias Stein |
這相當於大多數人希望在白天駕駛的距離,然後他們就有整晚可以進行充電。
這就是我們如何得出800公里(或是500英里這個不錯的數字)做為我們研發項目(R&D project)「Battery 500」的目標。該計畫在2009年始於加州聖荷西的IBM Almaden研究中心,並從那時開始,已成長為在歐洲、亞洲和美國的商業和學術參與者之間的跨國合作夥伴關係。它基於金屬空氣技術,在給定質量的情況下能包進比現今最先進技術的鋰離子電池更多的能量。我們雖已商業化多年,但我們的進展已足夠預測這些電池在可預見的未來中可以運用在車子上。為什麼我們這麼有信心?請繼續看下去。
電動馬達非常適合汽車供電。他們重量輕、非常有力(powerful)、效率超過90%、不需要複雜的傳輸,而且它產生的力矩恰到好處,可從0 rpm開始提供完全旋轉力。相較之下,內燃機除非以數千rpm旋轉,不然無法產生高力矩。
但是,即使是被一個接近理想的機構所推動,電動汽車有一個巨大的缺點,那就是電池的低能量含量。汽油每公斤約有13000 W·h,但最好的鋰離子電池僅存儲約250W·h/kg。再加上輔助電池設備,包括匯流條、冷卻系統以及電池管理系統,整個系統的能量密度又下降一半,使得電池的能量密度跟汽油原始能量密度相比只有可憐的1%。
汽油和電池的能量密度間的差距如此巨大,看似不可能做出有競爭力的電動車,然而Tesla Model S的成功卻已顯示它能夠做到。一個有利的主要因素是在輪子上,電動車在電池能量與動力間的高效率轉換—大約是美國所有以汽油為燃料的汽車的平均6倍。此外,電動汽車製造商放入他們能合理融入其設計最大、最重的電池,但即便如此仍遠遠達不到500英里的目標。結論是,電動車電池的能量密度要達到鋰離子電池的兩倍,才有辦法達成800公里的里程範圍。
在電極之中—或是之上
成本無論如何都與能量密度同樣重要。現今的電池每kW·h需要200~300元美金,這意味著,若給定平均範圍的5,6 km/kW·h,一輛以800公里為範圍的車將需要一顆150kW·h的電池,其要價30,000到45,000美元,相較之下BMW 2系列轎車的基本價格(base price)則為$33,000。如果此技術想獲得一個重要的立足點,每kW·h的價格至少要下降到100元以下。在這個價位上,當能源使用和保養等等運營成本大幅降低,與驅動這台靈敏的機器所帶來純粹的樂趣,將能確保其在市場上取得成功。
但是我們如何得到範圍800公里的電池呢?嗯,這得從當前最先進的鋰離子電池開始講起。
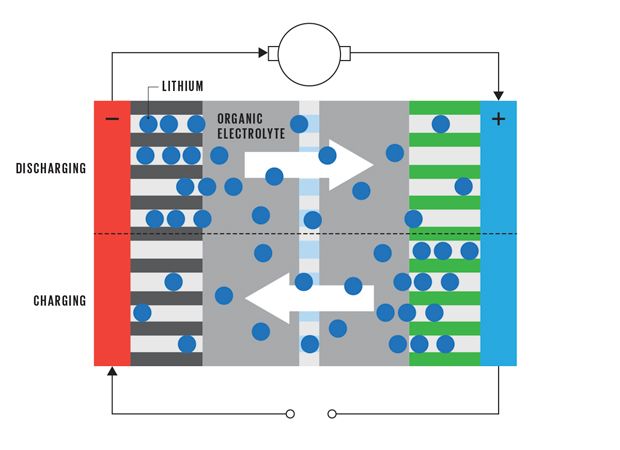
一個傳統的(或「嵌入(intercalation)」的)鋰離子電池是密封系統,該系統包含一個由石墨製成的電極(electrode)(陽極),和通常由過渡金屬的各種氧化物,如鈷、鎳或錳所製成的一個對置電極(陰極)。兩個電極都浸在溶有鋰鹽的有機電解液(liquid organic electrolyte)中。在電解液中,鋰離子從一個電極行進到另一個,方向根據電池是在充電還是放電。浸在電解質中的電極之間,有一個多孔聚合物(porous polymeric)隔板,用來防止電極之間短路。離子把自己插入電極材料的原子層之間。這個過程被稱為嵌入(intercalation),因為過程可逆(reversible),所以它允許充電。
如果電極透過外部電路連接,鋰離子將從負電極轉移到正電極,而電子流經所連接的外部電路,從而使電池放電;而外部施加的電壓將使離子流逆流,此時電池就能充電。電池容量取決於有多少材料可被嵌入。換句話說,電池容量與體積有關,即是陽極和陰極的質量。
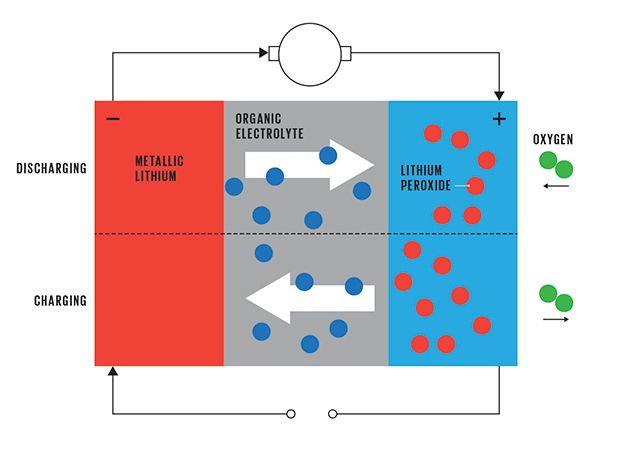
然而金屬空氣電池並不用嵌入,而是採用了一個正統(true)的電化學反應。為了更清楚的描述,我們假設金屬是鋰。在放電過程中,陽極的鋰金屬釋放鋰離子;這些離子通過電解質,然後和氧氣在陰極結合,形成過氧化鋰(Li2O2)。如同傳統的鋰離子電池,電子流過外部負載電路(load circuit)來補償(compensate)電池內部的鋰離子流動。過氧化物鋰累積在陰極多孔碳的表面上,在此參與反應的三方(鋰離子,電子,和氧)相遇並發生反應。因為反應發生在表面上,所以只要有廣大的表面積,陰極材料的體積或質量根本無關緊要。這也就是為何這種類型的電池,擁有如此高的能量密度最主要的原因。
不再那麼粗糙
裸金屬:鋰陽極在其原始狀態是平滑的。Photo:IBM
粗糙的材料:經過10次充放電循環時,鋰陽極的表面是粗糙的,顯示危險枝晶的生長。Photo:IBM
微小通道:當作者用奈米多孔隔板引導離子的流動時,鋰陽極在相同數目的週期後依然保持平滑。Photo:IBM
稱重和測量:IBM公司建立了這個質譜儀,通過質量來識別由鋰空氣電池中產生的氣體成分。Photo:IBM
甜甜圈:在該電子顯微鏡照片的反應中,過氧化鋰顯示為甜甜圈狀結構。Photo:IBM
充電則是反轉整件事的順序:外部施加的電壓打破過氧化鋰,氧經擴散回到環境中,而金屬離子回到陽極,在那裡他們得到電子,從而轉換回本體金屬(bulk metal)。
這個一般原則可以適用於多種不同的金屬。鋰-空氣、鉀-空氣和鈉-空氣—一位有趣的新競爭者[參見附文“Sodium: Less Energy, More Stability”(鈉:少能源,更穩定)]—都是可行的系統,因為他們適合(lend themselves to)充電。較重的金屬,如鋅、鎂、鐵、鋁已經證明很難充電,所以我們不會在這裡考慮它們。
我們的工作主要集中在鋰和鈉,讓我們從有更強能量存儲能力的鋰開始講起。太多外來(extraneous)的化學反應會在這些電池中亂搞了,為了理解這些副反應,我們精確地測量這些電池在循環過程中消耗和產生的氣體。對於這一點,我們使用了我們在IBM Almaden研究中心建立的一個複雜的電化學微分質譜儀(differential electrochemical mass spectrometer)。設有8個站測量平行實驗的氣體。
這台儀器帶給我們很重要的見解。例如,它顯示早期的鋰空氣電池充電時釋放的氧氣比放電時消耗的少得多。 (在大多數實驗中,我們用乾燥的氧氣而不是空氣。)
一個理想的電池,氧氣在放電過程中消耗的量應恰好等於充電時釋放的量。因此,我們的發現是個壞消息,因為它意味著充電時過氧化鋰(想得到)的解離過程中釋放的氧在攻擊電池本身的組件,特別是電解質。細胞並不是在充電—它們在自我毀滅!
在蘇黎世的IBM姊妹實驗室的幫助下,我們通過追踪實驗和計算機模擬這種寄生反應(parasitic reaction)的來源。我們認為其中的主要問題是有機電解質—它被破壞了。從那時起,我們已經走了朝向解決問題走了很長的路。當我們最新的電池充電時,我們的新電解液(稍後我們會描述它)使它們能夠釋放在放電過程中取得的大部分氧氣。我們也仔細監測電池在循環過程中產生的水和氫氣,因為它們的存在代表我們仍然見到至少一個其它寄生反應。
我們已經能達成200次的充放電循環,儘管到目前為止我們能做的只有限制放電小於理論最大值而已。
下面是一些我們的關鍵結論:
陽極:
鋰離子電池充電時,會有稱為枝晶(dendrite)的苔狀或樹狀結構形成,這些枝晶是危險的,因為它們會在陽極和陰極之間提供導電通路,可能使電池短路。而不同於標準鋰離子電池的石墨陽極(graphite anode),我們的鋰金屬表面在充電時會顯著改變其表面。透過在陽極和鋰離子的源極(source)之間放入特殊隔板,我們已經在限制枝晶的形成取得極大的成功。這個分離器有一層其中包含奈米級的孔—我們已嘗試了有機和無機材料。這些孔小到足以均勻地分佈流動離子的電流,從而抑制樹突的形成。藉由此奈米多孔隔板,金屬可維持光滑達數百週期,而使用標準隔板的電池僅過了幾個週期就形成樹突。另一種結合離子導電玻璃(ion-conducting glasses)與聚合物基質(polymer matrix)的膜甚至運作得更好。
幸運的是,電動汽車的大容量電池不需要幾千次的週期,幾百次即可。例如一台以500英里為範圍的汽車,若其一生要開過200,000英里(約320,000公里),僅需完全充電400次。
電解質:
我們使用的改進後電解質溶劑分子仍然可以被氧和其他操作期間產生的化合物分解。我們還沒有發現任何對具商業用途的鋰空氣電池足夠穩定的單一溶劑,但我們發現一些溶劑的混合(a cocktail of solvents)非常有效。陰極:
我們追蹤LiNO2(硝酸鋰)對碳陰極的影響,以盡量減少不良催化作用,如充電時電解質被加速破壞及釋放二氧化碳等。即使如此,該反應的充電電壓仍要高於700毫伏,高於電池的工作電壓。如此高的過電壓(overvoltge)會降低電池效率—意思是,只有一部份被充進電池的能量能在放電期間返回。雖然比你用普通碳素陰極(plain carbon cathode)得到的結果(超過1200毫伏)好多了,但它仍然太高,無法實際應用。當我們把碳換成金屬氧化物時也有類似的結果。催化劑:
對金屬空氣電池刻意使用催化劑的利弊已引起許多科學辯論。催化劑往往能明顯減少過電壓,但人們對淨效益必須格外謹慎,因為催化劑一般會加速電解質的破壞。此外,我們的理論研究表明,該鋰-氧的反應活化能(activation energy)在兩個方向都非常低,因此不應該需要催化劑。空氣處理:
我們稱這些裝置為鋰-空氣電池,但事實上我們已經大多採用乾燥氧氣。這裡要強調的是“乾燥”的,因為我們只需要從空氣中去除水蒸氣和二氧化碳,而不移除氮,才使其可用。若要做到商業規模的電池,我們需要投入大量工程努力,創造一個夠輕,高效,可靠的空氣淨化系統,以及保留這個技術的節能優勢。另一項傑出的工程任務是如何擴展到更大的電池,並將它們整合成一個多電池(multicell)模組和包裝,包括量身定制的電池管理系統。我們原來的電池長度約為13毫米、直徑約76毫米,我們正在測試長度與直徑皆100毫米的版本。
整個計畫都是由想達成高比能(specific energy)密度的慾望所驅使—比能即是每單位質量所具有的能量。那麼我們現在進展到哪了呢?
該鋰-氧反應具有理論(比能)能量密度的3,460 Wh/kg,這密度比化學上任何鋰離子的嵌入理論極限高得多。嵌入和金屬空氣化學(metal-air chemistries)的實際能量都比理論值低得多,因為電池組件貢獻的慣性質量(inert mass)並沒有參與反應,包括電解質,電池外殼,集流器,和隔板。另外,鋰-空氣電池還得包括電池用於準備外界空氣(ambient air)所需機械的慣性質量。正是這些工程問題與挑戰,成就了鋰空氣電池電動車的實際開發。
現在就引述鋰-氧技術的實際能量密度似乎言之過早,更何況是鋰空氣技術。這些數字取決於工程細節,且該計畫的重點仍然集中在材料和化學的基礎科學。然而早期的結果相當鼓舞人心,例如我們已經測量出陰極材料原始碳(raw carbon cathode material)的比能密度為15 kWh/kg(每克碳煙(carbon black)的能量相當於2.7伏特與5700 mAh的乘積)。但是正如我們前面所指出的,實際的能量密度將因為電池中其他組件的質量而大大降低。從電池的層次來看,我們目前估計可實際達成的最佳值約800 Wh/kg。
第一顆可實現的金屬空氣電池可能會用在公車、卡車和其他更能容納空氣清淨設備質量的大型車輛。但是,當技術觸及家用車,將其從今日電動車的「里程焦慮(range anxiety)」釋放,也把我們從對石油的依賴及其產生的問題中釋放,此時最深刻的變革將會到來。
鈉:少能源,更穩定
 |
| Illustration: Elias Stein |
能量較低反映了反應的性質,該反應僅使用一個電子,因此產生了超氧化鈉(NaO2)而非過氧化鈉(Na2O2)。這讓能量密度立即減低一半,該反應的理論比能為每公斤約1,100 watt-hours。
但另一方面,鈉空氣電池在充電上比鋰空氣電池更有效率,因為它們具有相對於700毫伏非常低的過電位(overpotential),低於20毫伏,因此有可能讓工作電壓保持在3伏特之下,從而保護組件遭到破壞性氧化,特別是在鋰空氣系統中觀察到的電解質破壞。我們藉由測量98%以上的效率證明了這一點。這些結果使其在循環過程中有良好的穩定性:在50次循環後,電池的容量基本上保持不變。
有幾個技術上的挑戰需要克服。例如,由於氧化的性質,鈉空氣電池要比鋰空氣當量吸入兩倍的空氣,活塞式發動機需要在相同功率下吸入更多氣流。然後金屬鈉的化學反應活性很高,你可能還記得在高中時見過,一小塊鈉與水發生了劇烈反應。
鋰較為罕見,而且不便宜,但是鈉和食鹽一樣普遍,而且不貴。鈉空氣電池的材料的成本可能會比鋰離子電池少十倍。從長遠來看,鋰金屬電池保證了最佳的性能,但有鑒於穩定、成本低及仍然令人印象深刻的比能等因素結合,鈉空氣技術可能有助於搭起連結今日的電池和遠處未來的橋–W.W.W. & H.-C. Kim
這篇文章將出現在2016年3月印刷出版為“The 800-km Battery.(800公里的電池)。”
關於作者
Winfried W. Wilcke,帶領IBM公司在加州聖荷西實驗室的奈米研究。
Ho-Cheol Kim領導該實驗室的先進能源存儲組。
來源:http://spectrum.ieee.org/transportation/advanced-cars/an-electric-car-battery-that-will-get-you-from-paris-to-brussels-and-back




